Blame
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 1 | --- |
| 2 | title: Hidrogénio |
|||
| 3 | author: |
|||
| 4 | - Diogo Ralha - 2021220818 |
|||
| 5 | - Raquel Bento - 2021222330 |
|||
| 6 | date: 2024-02-28 |
|||
| 7 | tags: #utilidades |
|||
| 8 | --- |
|||
| 9 | ||||
| e96137 | Nuno Oliveira | 2025-04-19 15:45:27 | 10 | # Hidrogénio |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 11 | |
| e96137 | Nuno Oliveira | 2025-04-19 15:45:27 | 12 | ## Introdução |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 13 | |
| 14 | A descoberta do hidrogénio remonta ao século XVI, embora só no século |
|||
| 15 | XVIII tenha sido identificado como um elemento distinto. Ao longo dos |
|||
| 16 | séculos, vários alquimistas e cientistas observaram a formação de um gás |
|||
| 17 | inflamável durante reações químicas, mas sem compreenderem a sua |
|||
| 18 | verdadeira natureza. |
|||
| 19 | ||||
| 20 | No século XVI, o alquimista e médico suíço Paracelso notou que, ao |
|||
| 21 | dissolver metais em ácidos, se libertava um gás. No entanto, sem o |
|||
| 22 | conhecimento necessário para interpretar esse fenómeno, não percebeu que |
|||
| 23 | se tratava de uma substância única. Mais tarde, no século XVII, o |
|||
| 24 | químico britânico Robert Boyle também documentou a libertação de um gás |
|||
| 25 | durante reações entre ácidos e metais, mas, tal como Paracelso, não o |
|||
| 26 | identificou como um elemento distinto. |
|||
| 27 | ||||
| 28 | Foi apenas em 1766 que o cientista britânico Henry Cavendish realizou |
|||
| 29 | experiências sistemáticas que permitiram uma melhor compreensão deste |
|||
| 30 | gás. Ao reagir diferentes metais com ácidos, recolheu o gás libertado e |
|||
| 31 | verificou que era significativamente mais leve do que o ar. Além disso, |
|||
| 32 | ao queimá-lo, observou que produzia água. Com base nestas |
|||
| 33 | características, designou-o como "ar inflamável", sendo o primeiro a |
|||
| 34 | reconhecer que se tratava de uma substância pura e não de um composto. |
|||
| 35 | No entanto, Cavendish não conseguiu determinar completamente a sua |
|||
| 36 | composição química. |
|||
| 37 | ||||
| 38 | A identificação definitiva do hidrogénio como elemento foi feita pelo |
|||
| 39 | químico francês Antoine Lavoisier, em 1783. Foi ele quem lhe deu o nome |
|||
| 40 | "hidrogénio", derivado dos termos gregos "hydro" (água) e "genes" |
|||
| 41 | (gerador), uma vez que demonstrou que a combustão do hidrogénio |
|||
| 42 | resultava na formação de água. <sup>\[1\]\ \[2\]\ \[3\]</sup> |
|||
| 43 | ||||
| 44 | A descoberta do hidrogénio representou um marco na química, contribuindo |
|||
| 45 | para o avanço da estequiometria, da teoria dos gases e da compreensão |
|||
| 46 | das reações químicas. Para além do seu impacto na ciência fundamental, o |
|||
| 47 | hidrogénio revelou-se essencial para diversas aplicações industriais e |
|||
| 48 | energéticas ao longo dos séculos. <sup>\[4\]</sup> |
|||
| 49 | ||||
| 50 | Atualmente, com o aumento da preocupação ambiental e a necessidade de |
|||
| 51 | transição energética, o hidrogénio tem ganho destaque como uma |
|||
| 52 | alternativa promissora aos combustíveis fósseis. Quando obtido a partir |
|||
| 53 | de fontes renováveis, o hidrogénio apresenta um elevado potencial para |
|||
| 54 | reduzir as emissões de carbono. A sua viabilidade deve-se, em grande |
|||
| 55 | parte, ao seu elevado rendimento energético, fornecendo cerca de 122 |
|||
| 56 | kJ/g, o que equivale a aproximadamente 2,75 vezes mais energia do que |
|||
| 57 | qualquer combustível fóssil convencional. <sup>\[5\]</sup> |
|||
| 58 | ||||
| 59 | Com o avanço das tecnologias de produção, armazenamento e utilização, o |
|||
| 60 | hidrogénio poderá desempenhar um papel crucial no futuro energético, |
|||
| 61 | promovendo um sistema mais sustentável e eficiente. |
|||
| 62 | ||||
| f25c62 | Raquel Alves | 2025-03-07 09:39:59 | 63 | 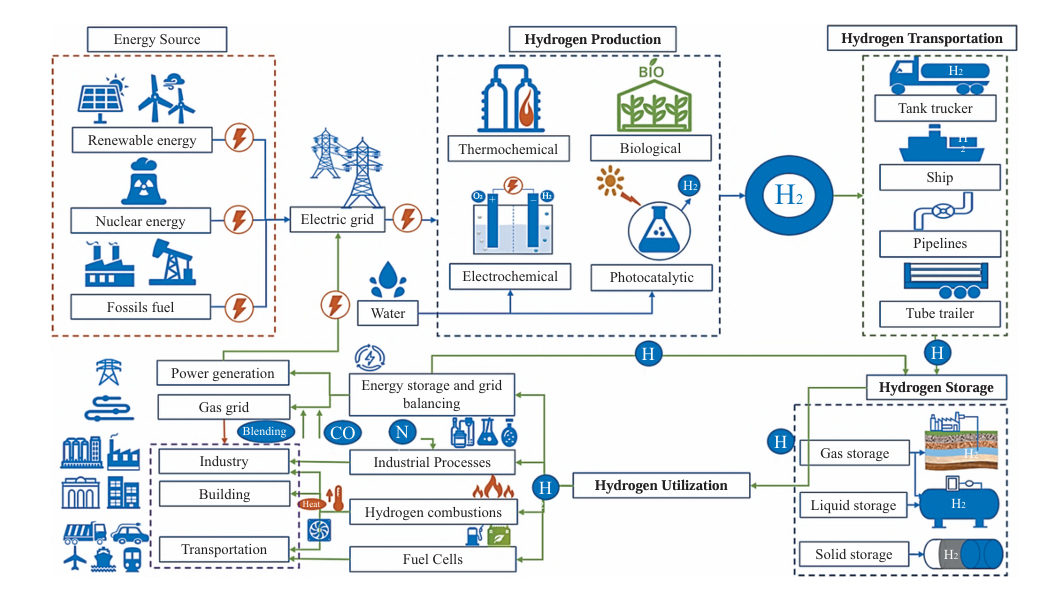 |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 64 | |
| 65 | **Figura 1**-Principais aplicações e formas de produção do hidrogénio |
|||
| 66 | <sup>\[6\]</sup> |
|||
| 67 | ||||
| f25c62 | Raquel Alves | 2025-03-07 09:39:59 | 68 | |
| 971f88 | Raquel Alves | 2025-03-07 10:02:27 | 69 | ## **O que é o hidrogénio?** |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 70 | |
| 71 | O hidrogénio (H), primeiro elemento da tabela periódica, é o mais |
|||
| 72 | simples e abundante no universo. Na sua forma mais comum, é composto por |
|||
| 73 | apenas um protão e um eletrão. No entanto, não ocorre naturalmente na |
|||
| 74 | sua forma molecular (H₂) em grandes quantidades, estando presente em |
|||
| 75 | compostos como a água e hidrocarbonetos. <sup>\[7\]\ \[8\]\ \[9\]</sup> |
|||
| 76 | ||||
| 77 | Entre as suas principais características, destacam-se: |
|||
| 78 | ||||
| 79 | - Leveza e baixa densidade: Gás mais leve do que a ar (cerca de 14 |
|||
| 80 | vezes), dissipando-se rapidamente na atmosfera. |
|||
| 81 | ||||
| 82 | - Estado físico e reatividade: Em condições normais, é um gás incolor, |
|||
| 83 | inodoro e insípido, altamente reativo e combustível. A sua molécula |
|||
| 84 | (H₂) é constituída por dois átomos de hidrogénio ligados por uma |
|||
| 85 | ligação covalente forte, conferindo-lhe uma certa estabilidade. |
|||
| 86 | ||||
| 87 | - Elevada energia específica: Possui um dos mais altos valores de |
|||
| 88 | energia específica, sendo promissor para a transição energética. |
|||
| 89 | ||||
| 90 | - Solubilidade e armazenamento: Baixa solubilidade em água e |
|||
| 91 | diferentes métodos de armazenamento, como compressão e liquefação. |
|||
| 92 | ||||
| 93 | Como é possível se visualizar na tabela 1, do ponto de vista |
|||
| 94 | termodinâmico, a forma atómica do hidrogénio apresenta entalpia e |
|||
| 95 | energia livre de Gibbs muito elevadas, enquanto a forma molecular (H₂) é |
|||
| 96 | mais estável e viável para armazenamento energético. Através da tabela |
|||
| 97 | 2, verifica-se que as propriedades físicas incluem baixa temperatura de |
|||
| 98 | fusão e ebulição, elevada condutividade térmica e viscosidade reduzida, |
|||
| 99 | tornando-o adequado para aplicações energéticas. |
|||
| 100 | ||||
| 101 | **Tabela 1**- Propriedades termodinâmicas do hidrogénio <sup>\[6\]</sup> |
|||
| 102 | ||||
| 103 | <table> |
|||
| 104 | <colgroup> |
|||
| 105 | <col style="width: 19%" /> |
|||
| 106 | <col style="width: 20%" /> |
|||
| 107 | <col style="width: 20%" /> |
|||
| 108 | <col style="width: 20%" /> |
|||
| 109 | <col style="width: 20%" /> |
|||
| 110 | </colgroup> |
|||
| 111 | <thead> |
|||
| 112 | <tr class="header"> |
|||
| 113 | <th><strong>Estado</strong></th> |
|||
| 114 | <th><p><strong>ΔH</strong></p> |
|||
| 115 | <p><strong>(kJ/mol)</strong></p></th> |
|||
| 116 | <th><p><strong>ΔG</strong></p> |
|||
| 117 | <p><strong>(kJ/mol)</strong></p></th> |
|||
| 118 | <th><p><strong>S</strong></p> |
|||
| 119 | <p><strong>(J/Kmol)</strong></p></th> |
|||
| 120 | <th><p><strong>Cp</strong></p> |
|||
| 121 | <p><strong>(J/Kmol)</strong></p></th> |
|||
| 122 | </tr> |
|||
| 123 | </thead> |
|||
| 124 | <tbody> |
|||
| 125 | <tr class="odd"> |
|||
| 126 | <td>H gasoso</td> |
|||
| 127 | <td>218,0</td> |
|||
| 128 | <td>203,3</td> |
|||
| 129 | <td>114,7</td> |
|||
| 130 | <td>20,8</td> |
|||
| 131 | </tr> |
|||
| 132 | <tr class="even"> |
|||
| 133 | <td>H2</td> |
|||
| 134 | <td>0</td> |
|||
| 135 | <td>0</td> |
|||
| 136 | <td>130,7</td> |
|||
| 137 | <td>28,8</td> |
|||
| 138 | </tr> |
|||
| 139 | </tbody> |
|||
| 140 | </table> |
|||
| 141 | ||||
| 142 | **Tabela 2**- Propriedades físicas do hidrogénio <sup>\[6\]</sup> |
|||
| 143 | ||||
| 144 | <table> |
|||
| 145 | <colgroup> |
|||
| 146 | <col style="width: 50%" /> |
|||
| 147 | <col style="width: 50%" /> |
|||
| 148 | </colgroup> |
|||
| 149 | <thead> |
|||
| 150 | <tr class="header"> |
|||
| 151 | <th><strong>Parâmetro</strong></th> |
|||
| 152 | <th><strong>Valor</strong></th> |
|||
| 153 | </tr> |
|||
| 154 | </thead> |
|||
| 155 | <tbody> |
|||
| 156 | <tr class="odd"> |
|||
| 157 | <td>Massa molar</td> |
|||
| 158 | <td>2, 016 g/mol</td> |
|||
| 159 | </tr> |
|||
| 160 | <tr class="even"> |
|||
| 161 | <td>Ponto de fusão</td> |
|||
| 162 | <td>13,8 K</td> |
|||
| 163 | </tr> |
|||
| 164 | <tr class="odd"> |
|||
| 165 | <td>Ponto de ebulição</td> |
|||
| 166 | <td>20,3 K</td> |
|||
| 167 | </tr> |
|||
| 168 | <tr class="even"> |
|||
| 169 | <td>Densidade do líquido a 24,2 K</td> |
|||
| 170 | <td>0,071 g/cm3</td> |
|||
| 171 | </tr> |
|||
| 172 | <tr class="odd"> |
|||
| 173 | <td>Densidade do sólido a 24,2K</td> |
|||
| 174 | <td>0,076 g/cm3</td> |
|||
| 175 | </tr> |
|||
| 176 | <tr class="even"> |
|||
| 177 | <td>Condutividade térmica a 25 ºC</td> |
|||
| 178 | <td>0,1805 W/mK</td> |
|||
| 179 | </tr> |
|||
| 180 | <tr class="odd"> |
|||
| 181 | <td>Capacidade calorifica a 25 ºC</td> |
|||
| 182 | <td>28,83 J/molK</td> |
|||
| 183 | </tr> |
|||
| 184 | <tr class="even"> |
|||
| 185 | <td>Calor de combustão a 25 ºC e 1 atm</td> |
|||
| 186 | <td>-285,829 kJ/mol</td> |
|||
| 187 | </tr> |
|||
| 188 | <tr class="odd"> |
|||
| 189 | <td>Temperatura de autoignição</td> |
|||
| 190 | <td>858 K</td> |
|||
| 191 | </tr> |
|||
| 192 | <tr class="even"> |
|||
| 193 | <td>Inflamabilidade no ar</td> |
|||
| 194 | <td>4-74%</td> |
|||
| 195 | </tr> |
|||
| 196 | </tbody> |
|||
| 197 | </table> |
|||
| 198 | ||||
| 199 | Como é possível observar-se na figura 1, o hidrogénio pode existir em |
|||
| 200 | vários estados dependendo da pressão e da temperatura. Pode ser |
|||
| 201 | armazenado como gás comprimido, líquido ou em compostos químicos. Os |
|||
| 202 | tanques de alta pressão atingem 70 MPa, enquanto os criogénicos operam a |
|||
| 203 | temperaturas muito baixas. Como combustível, tem uma relação |
|||
| 204 | energia/massa três vezes superior à gasolina, com elevada temperatura de |
|||
| 205 | ignição e chama mais quente. |
|||
| 206 | ||||
| f25c62 | Raquel Alves | 2025-03-07 09:39:59 | 207 | 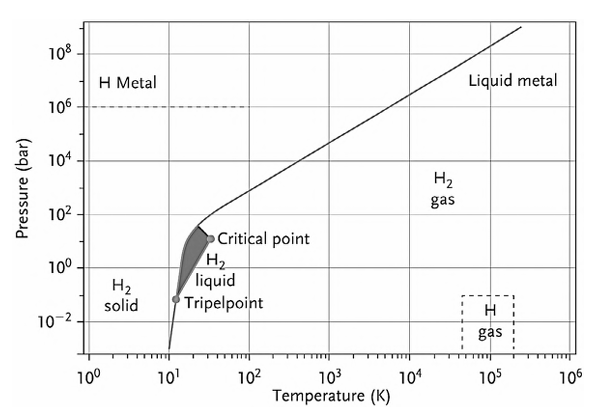 |
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 208 | |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 209 | **Figura 2**-Diagrama de fases do hidrogénio <sup>\[6\]</sup> |
| 210 | ||||
| 211 | A sua utilização exige estratégias rigorosas de segurança devido aos |
|||
| 212 | amplos limites de inflamabilidade e ao risco de ignição súbita. No |
|||
| 213 | entanto, a rápida dispersão no ar reduz a probabilidade de explosões em |
|||
| 214 | espaços abertos, tornando-o uma alternativa energética viável para um |
|||
| 215 | futuro sustentável. |
|||
| 216 | ||||
| f25c62 | Raquel Alves | 2025-03-07 09:39:59 | 217 | |
| 971f88 | Raquel Alves | 2025-03-07 10:02:27 | 218 | ## **Os tipos de hidrogénio** |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 219 | |
| 220 | O hidrogénio tem vindo a afirmar-se como uma alternativa viável, com |
|||
| 221 | capacidade para transformar vários setores industriais. A sua grande |
|||
| 222 | vantagem reside na versatilidade e no facto de, quando utilizado como |
|||
| 223 | fonte de energia, emitir exclusivamente vapor de água, tornando-se, |
|||
| 224 | assim, um elemento essencial na transição para um modelo económico mais |
|||
| 225 | sustentável. Contudo, a natureza do hidrogénio pode diferir |
|||
| 226 | substancialmente, dependendo da origem da energia empregue na sua |
|||
| 227 | produção e do respetivo impacto ambiental. |
|||
| 228 | ||||
| 229 | Atualmente, como é possível visualizar na tabela 3, são identificados |
|||
| 230 | dez tipos principais de hidrogénio: verde, azul, castanho, cinzento, |
|||
| 231 | rosa, roxo, turquesa, branco, vermelho e amarelo. |
|||
| 232 | <sup>\[10\]\ \[11\]\ \[12\]\ \[13\]</sup> |
|||
| 233 | ||||
| 234 | **Tabela 3**-Tipos de hidrogénio e os seus processos de obtenção |
|||
| 235 | <sup>\[6\]\ \[10\]\ \[11\]\ \[12\]\ \[13\]\ \[14\]</sup> |
|||
| 236 | ||||
| 237 | <table> |
|||
| 238 | <colgroup> |
|||
| 239 | <col style="width: 18%" /> |
|||
| 240 | <col style="width: 36%" /> |
|||
| 241 | <col style="width: 44%" /> |
|||
| 242 | </colgroup> |
|||
| 243 | <thead> |
|||
| 244 | <tr class="header"> |
|||
| 245 | <th><strong>Tipo de Hidrogénio</strong></th> |
|||
| 246 | <th><strong>Processo de obtenção</strong></th> |
|||
| 247 | <th><strong>Demonstração do processo de obtenção</strong></th> |
|||
| 248 | </tr> |
|||
| 249 | </thead> |
|||
| 250 | <tbody> |
|||
| 251 | <tr class="odd"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 252 | <td><strong>Hidrogénio Verde</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 253 | <td>É amplamente reconhecido como a opção mais ecológica, uma vez que é |
| 254 | gerado por eletrólise da água, utilizando energia proveniente de fontes |
|||
| 255 | renováveis, como a solar e a eólica. Este processo não gera emissões de |
|||
| 256 | carbono e faz uso de um recurso natural abundante. No entanto, enfrenta |
|||
| 257 | desafios como o alto custo de produção e a necessidade de infraestrutura |
|||
| 258 | específica.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 259 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image3.png" |
| 260 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 261 | </tr> |
| 262 | <tr class="even"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 263 | <td><strong>Hidrogénio Azul</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 264 | <td>A sua produção assenta na reforma do metano, um composto de origem |
| 265 | fóssil, mas diferencia-se pela utilização de tecnologias de captura e |
|||
| 266 | armazenamento de carbono (CCS), que permitem uma redução significativa |
|||
| 267 | das emissões poluentes. Embora não seja tão ecológico como o hidrogénio |
|||
| 268 | verde e a captura de carbono ainda não seja totalmente eficiente |
|||
| 269 | (podendo ocorrer fugas de CO<sub>2</sub>), este desempenha um papel |
|||
| 270 | importante no processo de descarbonização do setor energético.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 271 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image4.png" |
| 272 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 273 | </tr> |
| 274 | <tr class="odd"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 275 | <td><strong>Hidrogénio Castanho</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 276 | <td>Resulta da transformação de combustíveis fósseis (gaseificação), |
| 277 | como o carvão, sem qualquer mecanismo de retenção de carbono. O seu nome |
|||
| 278 | deriva precisamente da elevada carga poluente (CO<sub>2</sub> e gases |
|||
| 279 | nocivos) associada ao seu processo de produção.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 280 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image5.png" |
| 281 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 282 | </tr> |
| 283 | <tr class="even"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 284 | <td><strong>Hidrogénio Cinzento</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 285 | <td>É gerado através do método de reforma de metano a vapor (SMR), um |
| 286 | dos mais comuns na indústria do hidrogénio e, também, mais económico. |
|||
| 287 | Embora a sua pegada ambiental seja inferior à do hidrogénio castanho, |
|||
| 288 | continua a gerar emissões significativas de carbono.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 289 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image6.png" |
| 290 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 291 | </tr> |
| 292 | <tr class="odd"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 293 | <td><strong>Hidrogénio Rosa</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 294 | <td>Tem origem na eletrólise alimentada por energia nuclear. Além disso, |
| 295 | o calor residual das centrais nucleares pode ser aproveitado para |
|||
| 296 | otimizar a eficiência do processo. Como não envolve a emissão de gases |
|||
| 297 | com efeito de estufa, é considerado uma alternativa sustentável.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 298 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image7.png" |
| 299 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 300 | </tr> |
| 301 | <tr class="even"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 302 | <td><strong>Hidrogénio Roxo</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 303 | <td>É gerado através de eletrólise quimiotérmica, que combina |
| 304 | eletricidade e calor proveniente da energia nuclear. Este processo |
|||
| 305 | aumenta a eficiência de eletrólise, reduzindo o consumo elétrico |
|||
| 306 | necessário para a separação das moléculas de água. No entanto, a |
|||
| 307 | utilização de calor a temperaturas elevadas exige tecnologias avançadas, |
|||
| 308 | além de levantar desafios na gestão dos resíduos nucleares.</td> |
|||
| 309 | </tr> |
|||
| 310 | <tr class="odd"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 311 | <td><strong>Hidrogénio Vermelho</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 312 | <td>É produzido por meio de eletrólise de alta temperatura, utilizando o |
| 313 | calor de reatores nucleares de alta temperatura (HTGRs). Este método é |
|||
| 314 | considerado o mais eficiente em comparação com o hidrogénio rosa e o |
|||
| 315 | hidrogénio roxo, uma vez que reduz significativamente o consumo de |
|||
| 316 | eletricidade, tornando o processo mais económico a longo prazo. No |
|||
| 317 | entanto, a necessidade de reatores especializados e tecnologia avançada |
|||
| 318 | resulta em custos elevados e desafios tecnológicos na sua |
|||
| 319 | implementação.</td> |
|||
| 320 | </tr> |
|||
| 321 | <tr class="even"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 322 | <td><strong>Hidrogénio Turquesa</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 323 | <td>É produzido por pirólise do gás natural e tem como subproduto o |
| 324 | negro de fumo, uma forma sólida do carbono. Deste modo, não há emissão |
|||
| 325 | direta de <a href="https://www.ecycle.com.br/co2/">dióxido de |
|||
| 326 | carbono</a> na <a href="https://www.ecycle.com.br/co2/">atmosfera</a>. |
|||
| 327 | Porém, ainda é uma tecnologia emergente que requer um elevado consumo |
|||
| 328 | energético.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 329 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image8.png" |
| 330 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 331 | </tr> |
| 332 | <tr class="odd"> |
|||
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 333 | <td><strong>Hidrogénio Branco</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 334 | <td>É uma forma natural de hidrogénio encontrado de forma espontânea em |
| 335 | depósitos subterrâneos, podendo ser explorados através da perfuração de |
|||
| 336 | poços. A sua formação resulta de processos naturais, como a |
|||
| 337 | desgaseificação da crosta e do manto terrestre, reações químicas entre |
|||
| 338 | rochas e a interação com água e minerais, tornando-o numa potencial |
|||
| 339 | fonte sustentável de hidrogénio. No entanto, a sua disponibilidade é |
|||
| 340 | muito limitada.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 341 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image9.png" |
| 342 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 343 | <tr class="even"> |
| 855f91 | Nuno Oliveira | 2025-03-12 00:37:42 | 344 | <td><strong>Hidrogénio Amarelo</strong></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 345 | <td>É obtido através da fotoeletrólise com energia solar. É um processo |
| 346 | limpo, pois depende de uma fonte renovável de energia e não ocorrem |
|||
| 347 | emissões de CO<sub>2</sub>. Ainda assim, é um processo cujo preço é |
|||
| 348 | bastante elevado.</td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 349 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image10.png" |
| 350 | style="width:4in" /></td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 351 | </tr> |
| 352 | </tbody> |
|||
| 353 | </table> |
|||
| 354 | ||||
| 294b18 | Nuno Oliveira | 2025-03-09 11:51:22 | 355 | |
| 971f88 | Raquel Alves | 2025-03-07 10:02:27 | 356 | ## **Processos de obtenção de hidrogénio** |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 357 | |
| 358 | Os processos de produção de hidrogénio podem ser divididos entre duas |
|||
| 359 | grandes categorias: fontes fósseis (métodos baseados em combustíveis |
|||
| 360 | fósseis amplamente utilizados, mas com emissões significativas de |
|||
| 361 | dióxidos de carbono) e fontes renováveis (métodos renováveis |
|||
| 362 | sustentáveis, mas com desafios técnicos e económicos). |
|||
| 363 | ||||
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 364 | 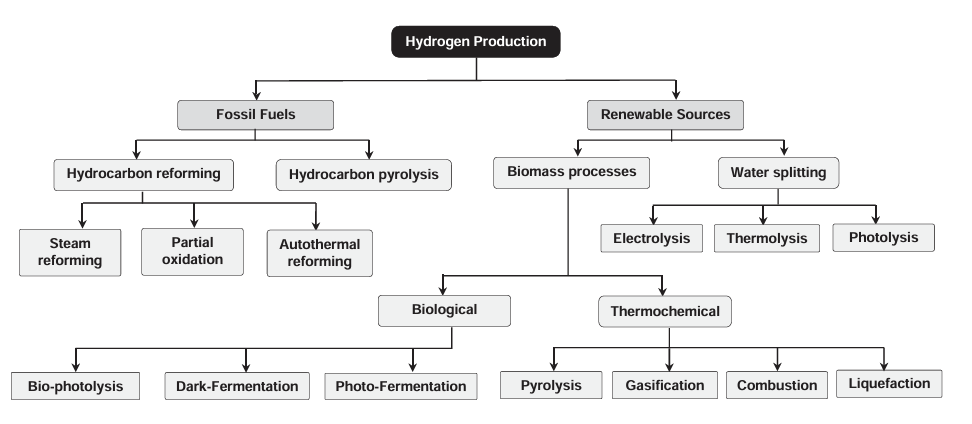 |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 365 | |
| 366 | **Figura 3**- Processos de produção de hidrogénio <sup>\[6\]</sup> |
|||
| 367 | ||||
| 368 | No caso das fontes fósseis, existem duas formas de obtenção de |
|||
| 369 | hidrogénio: a Reforma de Hidrocarbonetos que consiste na extração de |
|||
| 370 | hidrogénio de combustíveis fósseis, como o gás natural e que se divide |
|||
| 371 | em Reforma a Vapor de Metano (SMR), Oxidação Parcial (POX), Reforma |
|||
| 372 | Autotérmica (ATR); e a Pirólise de Hidrocarbonetos. <sup>\[6\]</sup> |
|||
| 373 | ||||
| 374 | **Tabela 4**-Processos de obtenção de hidrogénio a partir de fontes |
|||
| 375 | fósseis <sup>\[6\]\ \[15\]</sup> |
|||
| 376 | ||||
| 377 | <table> |
|||
| 378 | <colgroup> |
|||
| 379 | <col style="width: 12%" /> |
|||
| 380 | <col style="width: 30%" /> |
|||
| 381 | <col style="width: 57%" /> |
|||
| 382 | </colgroup> |
|||
| 383 | <thead> |
|||
| 384 | <tr class="header"> |
|||
| 385 | <th><strong>Processo</strong></th> |
|||
| 386 | <th><strong>Descrição do Processo</strong></th> |
|||
| 387 | <th><strong>Diagrama do Processo</strong></th> |
|||
| 388 | </tr> |
|||
| 389 | </thead> |
|||
| 390 | <tbody> |
|||
| 391 | <tr class="odd"> |
|||
| 392 | <td>Reforma a Vapor (SMR)</td> |
|||
| 393 | <td><p>O metano reage com vapor de água a altas temperaturas para |
|||
| 394 | produzir gás de síntese (mistura composta por hidrogénio e monóxido de |
|||
| 395 | carbono).</p> |
|||
| 396 | <p><u>Reações:</u></p> |
|||
| 397 | <p>Reforma do metano:</p> |
|||
| 398 | <p>CH<sub>4</sub> + H<sub>2</sub>O<span class="math inline">↔︎</span>CO + |
|||
| 399 | 3H<sub>2</sub></p> |
|||
| 400 | <p>Water-Gas Shift reaction (WGS):</p> |
|||
| 401 | <p>CO + H<sub>2</sub>O<span class="math inline">↔︎</span>CO<sub>2</sub> + |
|||
| 402 | H<sub>2</sub></p> |
|||
| 403 | <p>É um processo eficiente e amplamente utilizado na indústria. No |
|||
| 404 | entanto, gera emissões de dióxido de carbono e requer altas |
|||
| 405 | temperaturas.</p></td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 406 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image12.png" |
| 91130a | Nuno Oliveira | 2025-03-12 00:29:14 | 407 | style="width:5in" /></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 408 | </tr> |
| 409 | <tr class="even"> |
|||
| 410 | <td>Oxidação Parcial (POX)</td> |
|||
| 411 | <td><p>O hidrocarboneto é parcialmente oxidado para produzir gás de |
|||
| 412 | síntese.</p> |
|||
| 413 | <p><u>Reações:</u></p> |
|||
| 414 | <p>CH<sub>4</sub> + 1/2O<sub>2</sub> <span class="math inline">↔︎</span> |
|||
| 415 | CO + 2 H<sub>2</sub></p> |
|||
| 416 | <p>CH<sub>4</sub> + 2O<sub>2</sub><span class="math inline">↔︎</span> |
|||
| 417 | CO<sub>2</sub> + 2 H<sub>2</sub>O</p> |
|||
| 418 | <p>Este processo é rápido e adequado para hidrocarbonetos pesados. Ainda |
|||
| 419 | assim produz menos hidrogénio que a reforma a vapor e gera dióxido de |
|||
| 420 | carbono.</p></td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 421 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image13.png" |
| 91130a | Nuno Oliveira | 2025-03-12 00:29:14 | 422 | style="width:5in" /></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 423 | </tr> |
| 424 | <tr class="odd"> |
|||
| 425 | <td>Reforma Autotérmica (ATR)</td> |
|||
| 426 | <td><p>É a combinação da Reforma a Vapor e Oxidação Parcial, sendo |
|||
| 427 | utilizado calor gerado internamente ao processo.</p> |
|||
| 428 | <p><u>Reação:</u></p> |
|||
| 429 | <p>4CH<sub>4</sub> + O<sub>2</sub> + 2H<sub>2</sub>O<span |
|||
| 430 | class="math inline">↔︎</span> 4CO + 10H<sub>2</sub></p> |
|||
| 431 | <p>Apresenta maior eficiência energética do que a reforma a vapor |
|||
| 432 | isolada, mas é um processo mais complexo e necessita de controlo preciso |
|||
| 433 | das reações envolventes.</p></td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 434 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image14.png" |
| 3a0022 | Nuno Oliveira | 2025-03-12 00:29:52 | 435 | style="width:5in" /></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 436 | </tr> |
| 437 | <tr class="even"> |
|||
| 438 | <td>Pirólise</td> |
|||
| 439 | <td><p>Corresponde à decomposição térmica dos hidrocarbonetos em |
|||
| 440 | hidrogénio e carbono sólido, sem emissões diretas de dióxido de |
|||
| 441 | carbono.</p> |
|||
| 442 | <p><u>Reação:</u></p> |
|||
| 443 | <p>CH<sub>4</sub> <span class="math inline">→</span> C + |
|||
| 444 | 2H<sub>2</sub></p> |
|||
| 445 | <p>Este processo promove a redução de emissões de gases de efeito de |
|||
| 446 | estufa (GEE), mas necessita de tecnologias que se encontram em |
|||
| 447 | desenvolvimento e ainda de altas temperaturas de operação.</p></td> |
|||
| 4eb8da | Nuno Oliveira | 2025-03-12 00:27:49 | 448 | <td> <img src="/Utilidades%20industriais/Gases%20industriais/Hidrog%C3%A9nio/./image15.png" |
| 91130a | Nuno Oliveira | 2025-03-12 00:29:14 | 449 | style="width:5in" /></td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 450 | </tbody> |
| 451 | </table> |
|||
| 452 | ||||
| 453 | Através de fontes renováveis, é possível optar-se por processos com |
|||
| 454 | biomassa (métodos que utilizam matéria orgânica como fonte de |
|||
| 455 | hidrogénio) ou pela separação da água (*Water Splitting*), ou seja, |
|||
| 456 | métodos que envolvem a quebra de moléculas de água para extrair |
|||
| 457 | hidrogénio. |
|||
| 458 | ||||
| 459 | Os Processos com Biomassa podem dividir-se em métodos biológicos, isto |
|||
| 460 | é, processos naturais com baixo impacto ambiental, mas apresentam uma |
|||
| 461 | baixa eficiência e tecnologias em desenvolvimento, e em métodos |
|||
| 462 | termoquímicos, ou seja, processos que promovem a redução de resíduos |
|||
| 463 | orgânicos e as baixas ou neutras emissões de carbono. No entanto, a sua |
|||
| 464 | eficiência é variável consoante o processo e requer grandes quantidades |
|||
| 465 | de biomassa. |
|||
| 466 | ||||
| 467 | Os Processos de Separação de Água podem dividir-se entre a eletrólise, a |
|||
| 468 | termólise e a fotólise. |
|||
| 469 | ||||
| 470 | **Tabela 5**-Processos de obtenção de hidrogénio a partir de fontes |
|||
| 471 | renováveis <sup>\[6\]\ \[15\]</sup> |
|||
| 472 | ||||
| 473 | <table> |
|||
| 474 | <colgroup> |
|||
| 475 | <col style="width: 33%" /> |
|||
| 476 | <col style="width: 33%" /> |
|||
| 477 | <col style="width: 33%" /> |
|||
| 478 | </colgroup> |
|||
| 479 | <thead> |
|||
| 480 | <tr class="header"> |
|||
| 481 | <th colspan="2"><strong>Processos com Biomassa</strong></th> |
|||
| 482 | <th rowspan="2"><strong>Processos por separação de água (<em>Water |
|||
| 483 | Splitting</em>)</strong></th> |
|||
| 484 | </tr> |
|||
| 485 | <tr class="odd"> |
|||
| 486 | <th><strong>Métodos Biológicos</strong></th> |
|||
| 487 | <th><strong>Métodos Termoquímicos</strong></th> |
|||
| 488 | </tr> |
|||
| 489 | </thead> |
|||
| 490 | <tbody> |
|||
| 491 | <tr class="odd"> |
|||
| 492 | <td><p><u>Biofotólise</u>: Certas algas e bactérias utilizam a luz para |
|||
| 493 | quebrar moléculas de água e formar a molécula de hidrogénio.</p> |
|||
| 494 | <p><u><em>Dark-Fermentation</em>:</u> Os microrganismos fermentam |
|||
| 495 | substratos orgânicos e produzem hidrogénio.</p> |
|||
| 496 | <p><u>Foto-Fermentação:</u> As bactérias fotossintéticas convertem |
|||
| 497 | biomassa em hidrogénio.</p></td> |
|||
| 498 | <td><p><u>Pirólise:</u> Consiste na decomposição térmica da biomassa |
|||
| 499 | para gerar hidrogénio.</p> |
|||
| 500 | <p><u>Gaseificação:</u> Conversão da biomassa em gás de síntese a altas |
|||
| 501 | temperaturas.</p> |
|||
| 502 | <p><u>Combustão:</u> A biomassa é queimada para gerar energia com |
|||
| 503 | formação de gases.</p> |
|||
| 504 | <p><u>Liquefação:</u> Ocorre a transformação da biomassa em óleo |
|||
| 505 | líquido, que pode ser processado para obtenção de hidrogénio.</p></td> |
|||
| 506 | <td><p><u>Eletrólise:</u> Utiliza a eletricidade para decompor moléculas |
|||
| 507 | de água em hidrogénio e oxigénio. É um processo com zero/baixas emissões |
|||
| 508 | de dióxido de carbono, dependendo do tipo de energia utilizada. No |
|||
| 509 | entanto é de alto consumo energético e custo elevado.</p> |
|||
| 510 | <p><u>Termólise:</u> Ocorre a decomposição térmica as moléculas de água |
|||
| ebbea6 | Diogo Ralha | 2025-03-07 10:00:14 | 511 | em hidrogénio e oxigénio a temperaturas superiores a 2500ºC. |
| 512 | É um processo direto sem necessidade de reagentes, mas requer temperaturas extremamente elevadas e materiais resistentes ao |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 513 | calor.</p> |
| 514 | <p><u>Fotólise:</u> Utiliza a energia solar para decompor as moléculas |
|||
| 515 | de água hidrogénio e oxigénio. Deste modo, é considerado um processo |
|||
| 516 | sustentável e limpo. Contudo as tecnologias ainda se encontram em |
|||
| 517 | estágio inicial e eficiência baixa.</p></td> |
|||
| 518 | </tr> |
|||
| 519 | </tbody> |
|||
| 520 | </table> |
|||
| 521 | ||||
| 294b18 | Nuno Oliveira | 2025-03-09 11:51:22 | 522 | |
| 971f88 | Raquel Alves | 2025-03-07 10:02:27 | 523 | ## **Aplicações do Hidrogénio** |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 524 | |
| 525 | O hidrogénio é um elemento versátil com diversas aplicações na |
|||
| 526 | indústria, energia e transporte. Com o crescente interesse na |
|||
| 527 | descarbonização, o hidrogénio tem sido explorado como uma alternativa |
|||
| 528 | sustentável para reduzir emissões de dióxido de carbono e melhorar a |
|||
| 529 | eficiência energética em vários setores. |
|||
| 530 | ||||
| 531 | O armazenamento do hidrogénio é um desafio fundamental para a sua |
|||
| 532 | aplicação em diversos setores. Cada tipo de aplicação de hidrogénio |
|||
| 533 | requer um método de armazenamento diferente, tendo como base certos |
|||
| 534 | fatores como a segurança, a viabilidade económica e facilidade de |
|||
| 535 | transporte. |
|||
| 536 | ||||
| 537 | **Tabela 6**-Métodos de Armazenamento de hidrogénio |
|||
| 538 | <sup>\[6\]\ \[15\]</sup> |
|||
| 539 | ||||
| 540 | <table> |
|||
| 541 | <colgroup> |
|||
| 542 | <col style="width: 16%" /> |
|||
| 543 | <col style="width: 51%" /> |
|||
| 544 | <col style="width: 32%" /> |
|||
| 545 | </colgroup> |
|||
| 546 | <thead> |
|||
| 547 | <tr class="header"> |
|||
| 548 | <th rowspan="2"><strong>Estado Gasoso</strong></th> |
|||
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 549 | <td><p><u>Armazenamento em Alta Pressão (<em>Compressed Hydrogen |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 550 | Storage</em>)</u>:</p> |
| 551 | <p>O hidrogénio é comprimido a pressões elevadas (350-700 bar) e |
|||
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 552 | armazenado em cilindros metálicos ou tanques de compósitos.</p></td> |
| 553 | <td><u>Motivo:</u> Uso em transporte e abastecimento rápido (usado em |
|||
| 554 | veículos - FCEVs).</td> |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 555 | </tr> |
| 556 | <tr class="odd"> |
|||
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 557 | <td><p><u>Armazenamento em Cavidades Geológicas:</u></p> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 558 | <p>O hidrogénio é armazenado em reservatórios subterrâneos (por exemplo, |
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 559 | formações geológicas).</p></td> |
| 560 | <td><u>Motivo:</u> Armazenamento em larga escala, ideal para gestão de |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 561 | energia renovável (reservatórios estratégicos para redes elétricas |
| 0233a7 | Raquel Alves | 2025-03-07 09:54:19 | 562 | baseadas em hidrogénio).</td> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 563 | </tr> |
| 564 | </thead> |
|||
| 565 | <tbody> |
|||
| 566 | <tr class="odd"> |
|||
| c19a7a | Raquel Alves | 2025-03-07 09:55:48 | 567 | <th><strong>Estado Líquido</strong></th> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 568 | <td><p><em><u>Cryogenic Hydrogen Storage:</u></em></p> |
| 569 | <p>O hidrogénio arrefecido a -253ºC e mantido em tanques |
|||
| 570 | criogénicos.</p></td> |
|||
| 571 | <td><u>Motivo:</u> Essencial para aplicações espaciais e transportes de |
|||
| 572 | longo alcance (indústria aeroespacial - combustível para |
|||
| 573 | foguetões).</td> |
|||
| 574 | </tr> |
|||
| 575 | <tr class="even"> |
|||
| c19a7a | Raquel Alves | 2025-03-07 09:55:48 | 576 | <th rowspan="3"><strong>Armazenamento em Materiais Sólidos</strong></th> |
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 577 | <td><p><u>Hidretos Metálicos <em>(Metal Hydrites)</em>:</u></p> |
| 578 | <p>O hidrogénio reage com metais (por exemplo, magnésio) e forma |
|||
| 579 | hidretos reversíveis.</p></td> |
|||
| 580 | <td><u>Motivo:</u> Aplicações em sistemas estacionários e militares, |
|||
| 581 | devido à sua segurança.</td> |
|||
| 582 | </tr> |
|||
| 583 | <tr class="odd"> |
|||
| 584 | <td><p><u>Materiais Adsorventes (MOFs e Carvão ativado):</u></p> |
|||
| 585 | <p>O hidrogénio é armazenado em materiais porosos, o que promove o |
|||
| 586 | aumento da massa volumétrica.</p></td> |
|||
| 587 | <td><u>Motivo:</u> Potencial para armazenamento eficiente a baixas |
|||
| 588 | pressões para a pesquisa e desenvolvimento de baterias de |
|||
| 589 | hidrogénio.</td> |
|||
| 590 | </tr> |
|||
| 591 | <tr class="even"> |
|||
| 592 | <td><p><u><em>Liquid Organic Hydrogen Carries</em> – LOHC:</u></p> |
|||
| 593 | <p>O hidrogénio é armazenado em moléculas líquidas orgânicas (por |
|||
| 594 | exemplo, tolueno e dibenziltolueno - DBT) que podem ser hidrogenadas e |
|||
| 595 | desidrogenadas reversivelmente.</p></td> |
|||
| 596 | <td><u>Motivo:</u> Promove a segurança e facilidade de transporte de |
|||
| 597 | hidrogénio.</td> |
|||
| 598 | </tr> |
|||
| 599 | </tbody> |
|||
| 600 | </table> |
|||
| 601 | ||||
| 294b18 | Nuno Oliveira | 2025-03-09 11:51:22 | 602 | |
| 603 | ## Referências |
|||
| 505810 | Raquel Alves | 2025-03-06 10:21:19 | 604 | |
| 605 | \[1\]-<https://chem.libretexts.org/Bookshelves/Inorganic_Chemistry/Chemistry_of_the_Main_Group_Elements_(Barron)/02%3A_Hydrogen/2.01%3A_Discovery_of_Hydrogen> |
|||
| 606 | (acedido em fevereiro de 2025) |
|||
| 607 | ||||
| 608 | \[2\]- <https://www.metallurgyfordummies.com/history-of-hydrogen.html> |
|||
| 609 | (acedido em fevereiro de 2025) |
|||
| 610 | ||||
| 611 | \[3\]- |
|||
| 612 | <https://www.mwcog.org/file.aspx?&A=zkpv0NhzZDWLPqP7LLLYTPZMIgxuq1QGhT8%2BMkINPbo%3D> |
|||
| 613 | (acedido em fevereiro de 2025) |
|||
| 614 | ||||
| 615 | \[4\]- Tian Q., Yao S., Shao M., Zhang W., Wang H., |
|||
| 616 | Origin, discovery, exploration and development status and prospect of global natural |
|||
| 617 | hydrogen under the background of “carbon neutrality”, China Geology, |
|||
| 618 | 2022 (acedido em fevereiro de 2025) |
|||
| 619 | ||||
| 620 | \[5\]- Balat, M. (2008). Potential importance of hydrogen as a future |
|||
| 621 | solution. International Journal of Hydrogen Energy, 4013-4029 (acedido |
|||
| 622 | em fevereiro de 2025) |
|||
| 623 | ||||
| 624 | \[6\]- Merouani - Hydrogen Production, Storage and Utilization, de |
|||
| 625 | Gruyter, 2025 (acedido em fevereiro de 2025) |
|||
| 626 | ||||
| 627 | \[7\]-.<https://energyeducation.ca/encyclopedia/Molecular_hydrogen> |
|||
| 628 | (acedido em fevereiro de 2025) |
|||
| 629 | ||||
| 630 | \[8\]-<https://periodic-table.rsc.org/element/1/hydrogen> (acedido em |
|||
| 631 | fevereiro de 2025) |
|||
| 632 | ||||
| 633 | \[9\]-<https://www.britannica.com/science/hydrogen> (acedido em |
|||
| 634 | fevereiro de 2025) |
|||
| 635 | ||||
| 636 | \[10\]-<https://energyeducation.ca/encyclopedia/Types_of_hydrogen_fuel> |
|||
| 637 | (acedido em fevereiro de 2025) |
|||
| 638 | ||||
| 639 | \[11\]-<https://stargatehydrogen.com/blog/types-of-hydrogen/> (acedido |
|||
| 640 | em fevereiro de 2025) |
|||
| 641 | ||||
| 642 | \[12\]-<https://www.brunel.net/en/blog/renewable-energy/3-main-types-of-hydrogen> |
|||
| 643 | (acedido em fevereiro de 2025) |
|||
| 644 | ||||
| 645 | \[13\]-<https://hydrogeneurope.eu/in-a-nutshell/> (acedido em fevereiro |
|||
| 646 | de 2025) |
|||
| 647 | ||||
| 648 | \[14\]-<https://www.upscprep.com/types-of-hydrogen-green-purple-pink-yellow-bluw-turquoise-grey-brown-black-upsc-current-affairs/> |
|||
| 649 | (acedido em fevereiro de 2025) |
|||
| 650 | ||||
| 651 | \[15\]- Farinha J. Reformação de metano com vapor de água em reformador |
|||
| 652 | de escala laboratorial, Instituto Superior Técnico, 2008 |
|||
| 653 | <https://fenix.tecnico.ulisboa.pt/downloadFile/395137864141/Mestrado_Jos%E9_Farinha.pdf> |
|||
| 654 | (acedido em fevereiro de 2025) |
